Оптимизация качественного и количественного состава питательных сред для глубинного культивирования Pleurotus ostreatus
Разработаны и оптимизированы питательные среды для глубинного культивирования гриба Pleurotus ostreatus Р-27 (штамм 439): Amycel 3000 на основе крахмалосодержащих побочных продуктов мукомольной промышленности и различных источников азота. Для промышленного использования предложено применение глютена с концентрацией 30% или неразбавленного соевого молока, с концентрацией 50%, в качестве источников азота, при одновременном применении овсяных или ржаных гидролизатов, с концентрацией сахаров 0,5%, что дает возможность получать сухую биомассу мицелия в количестве примерно 40-50 г / л.
Введение
На сегодняшний день остается нерешенной проблема дефицита и качества белковых продуктов, а в ряде стран мира проблема «белкового голодания». Промышленная микология является перспективным направлением биотехнологии и способна помочь в решении этих проблем. Получение грибной биомассы в условиях глубинного культивирования при создании оптимальных условий выращивания и оптимизации состава питательной среды является дешевым и доступным способом получения высококачественного экологического белка пищевого и кормового назначения, обогащенного незаменимыми аминокислотами, и быстрым способом получения в больших количествах посевными мицелия при выращивании плодовых тел [1 , 2]. Наиболее исследуемый объект промышленной микологии — высшей съедобный гриб вешенка обыкновенная. К преимуществам грибов рода Pleurotus относят высокую скорость роста мицелия, значительную конкурентоспособность по отношению к посторонней микрофлоры и способность утилизировать различные растительные отходы сельского хозяйства и промышленности [3].
Существующие исследования по искусственному выращиванию грибов направленные на увеличение выхода целевых продуктов (биомассы, белка, аминокислот) [1, 2, 4], создание грибного аромата [5] и разработку новых относительно дешевых и простых питательных сред. Вариантами решения этих проблем могут быть поиск или создание новых промышленных штаммов грибов [1, 6] и оптимизация качественного и количественного состава питательных сред для выращивания широко применяемых в промышленности штаммов, например Pleurotus ostreatus [4]. Решение данных задач также способствует решению другой важной проблемы, а именно утилизации существующих отходов сельского-хозяйства и пищевой промышленности. Достаточно нерационально используются крахмалосодержащие отходы растениеводства, в том числе побочные продукты и отходы мукомольной промышленности. К тому же, количество растительных отходов в несколько раз превышает долю целевой полученной продукции. При этом, потенциально возможные доходы от реализации продукции, полученной из различных отходов, могут быть значительно большими, чем доходы от продажи основного продукта и позволят без дополнительных затрат на выращивание зерна поднять общую рентабельность производства. Отходы зерноперерабатывающей промышленности и сельского хозяйства безвредны, легко поддаются ферментативной и микробиологической биоконверсии и широко используются как сырье в кормопроизводстве [7]. Но такой способ утилизации подобных отходов отличается низкой эффективностью. Невесомая кормовая ценность данных отходов объясняется высоким содержанием сложных полисахаридов, малым количеством перевариваемого белка и незаменимых аминокислот. Альтернативным способом утилизации крахмалосодержащие растительных отходов и побочных продуктов зернопереработки является использование их для глубинного культивирования мицелиальных организмов (например Pleurotus ostreatus) с целью получения качественных белковых продуктов пищевого и кормового назначения.
Зерновые отходы требуют перевода их полисахаридных комплексов в легко усваиваемые ди-и моносахариды, путем кислотного или ферментативного гидролиза [8]. Предварительная обработка сырья непосредственно способствует увеличению выхода мицелия и содержания белка в нем. Кислотный гидролиз происходит при участии серной, соляной или ортофосфорной кислоты и имеет ряд недостатков: загрязнение токсичными продуктами гидролиза исследовательской биомассы продуцента и конечного продукта, наличие вредных отходов. Ферментативный гидролиз, связанный с действием ферментных препаратов, является экологическим процессом и наоборот, имеет ряд преимуществ: отсутствие загрязнения биомассы продуцента и конечного продукта, довольно небольшие затраты ферментного препарата (по отношению к количеству субстрата) невысокая стоимость ферментных препаратов, проведение гидролиза за мягких условиях без значительных энергозатрат и вовлечения в процесс дополнительно дорогостоящего оборудования; направленность процесса — образуются простые углеводы, которые могут непосредственно усваиваться продуцентом.
Таким образом, подбор и оптимизация питательных сред для глубинного культивирования высших съедобных грибов остается актуальной проблемой. В связи с этим, целью данной работы является разработка и оптимизация состава питательных сред на основе гидролизатов крахмалосодержащие компонентов и различных источников азота для выращивания гриба Pleurotus ostreatus.
Материал и методика исследований
В данных опытах использовали культуру гриба Pleurotus ostreatus Р-27 (штамм 439): Amycel 3000, отличающийся высокой урожайностью [3], были применены среды, которые вмещали в качестве источника углерода ферментные гидролизаты побочных продуктов переработки ржи и овса, в качестве источника азота отходы крахмалопаточного производства — глютен или продукты переработки сои — соевое молоко. Для приготовления контрольных сред использовали другие отходы крахмалопаточного производства — зеленую патоку и кукурузный экстракт в качестве источников углерода и азота соответственно. Выращивание грибной биомассы проводили по стадийно. Музейный культуру продуцента хранили на сусло-агаровой среде, посевными культуру выращивали на агаризованной среде вмещало отвар пшеницы. Ферментацию проводили на жидких питательных средах. Контрольный среду вмещало 6% кукурузного экстракта, что соответствует 0,24%-й концентрации азота и 5% зеленой патоки, что соответствует 0,15%-й концентрации углеводов. Для приготовления опытных сред использовали в качестве источника углерода жидкие ферментные гидролизаты побочных продуктов мукомольной промышленности (ржаные или овсяные) в объемных концентрациях 38; 13; 4%, что соответствует концентрациям сахаров 1,50; 0,50; 0,15% соответственно . В качестве источника азота использовали глютен с объемными концентрациями 20, 30; 40; 50%, что соответствует концентрациям азота 0,16; 0,24; 0,32; 0,40% или соевое молоко с объемными концентрациями 20; 50; 85%, что соответствует концентрациям азота 0,11; 0,22; 0,43%. Контрольный и опытные среды также помещали 0,05% KH2PO4, 2% кукурузного масла, pH = 6,9-7. Таким образом, концентрация азота в контрольную среде (6% кукурузного экстракта) и опытных средах с глютеном (30%) или соевым молоком (50%) примерно одинакова и составляет 0,22-0,24%.
Глубинное культивирование проводили в течение 5 суток при температуре 26-28 º С и режиме перемешивания 200-240 об / мин на микробиологических термостатных качалках УВМТ-12-250 в колбах емкостью 250 мл, с объемом питательной среды 50 мл. Культуру гриба, выросшей в процессе ферментации, отделяли от культуральной жидкости центрифугированием при 3000 об / мин. 10 минут на центрифуге Т-23. Сырую биомассу гриба высушивали при температуре 105 º С до постоянного веса. Для обработки крахмалосодержащие отходов применяли отечественные промышленные ферментные препараты микробного происхождения «Альфалад БН» (α-амилаза Гх-466) и «Глюколад» (глюкоамилаза ГЗх-1) Ладыжинского завода. Выбор препаратов связан с известной спецификой их воздействия на углеродные компоненты. Препарат амилолитической действия — α-амилаза (1:1000, активность 1900 ед / мл) расщепляет α-1 ,4-глюкозидные связи с образованием нормальных α-декстринов, глюкозы, мальтозы. Глюкоамилаза (1:200, активность 5800 ед / мл) расщепляет α-1, 4 — и α-1 ,6-глюкозидные связи с образованием глюкозы в качестве продукта гидролиза. Количество повторов исследования составила 10. Полученные результаты обрабатывали методом математической статистики [9].
Результаты исследований и обсуждение
В проведенном исследовании для выращивания гриба Pleurotus ostreatus осуществили подбор основного сырья, а именно источников углерода, полученных ферментативным гидролизом побочных крахмалосодержащие продуктов, которые накапливаются при перемалывании зерна в муку. Оптимизировали концентрацию сахаров в полученных гидролизата (табл.1). В качестве исследовательского источника азота применяли глютен (30%), контрольного — кукурузный экстракт (6%). Оптимальная концентрация глютена была установлена в отдельном исследовании.
Таблица 1 – Определение оптимальной концентрации сахаров для выращивания гриба Pleurotus ostreatus на питательных средах с гидролизатами побочных продуктов овсяной и ржаной муки глютеном (30%)
| Источники углерода и азота | Концентрация сахаров,% | Количество сухой биомассы, г/100 мл * |
| Зеленая патока и кукурузный экстракт | 0,15 | 1,977 ± 0,098 |
| Овсяный гидролизат и глютен | 1,5 | 4,569 ± 0,228 |
| 0,5 | 4,339 ± 0,216 | |
| 0,15 | 3,458 ± 0,172 | |
| Ржаной гидролизат и глютен | 1,5 | 4,774 ± 0,238 |
| 0,5 | 4,488 ± 0,224 | |
| 0,15 | 3,765 ± 0,188 |
* — Данные представлены в виде x ± m • t0,05, где x — среднее арифметическое, m — ошибка среднего арифметического, t0,05 — коэффициент Стьюдента на уровне значимости 0,05.
Все исследовательские концентрации углеводов вызвали увеличение количества биомассы более чем на 80% по сравнению с контролем. Было определено, что лучших результатов, примерно в 2 — 2,5 раза больше по сравнению с контролем, достигли при применении овсяной или ржаной гидролизата, в которых концентрация сахаров составляла 0,5% и 1,5% соответственно. Достоверных различий в накоплении биомассы продуцентом на опытных средах с овсяными и ржаными гидролизатами данным концентрациями сахаров (0,5 и 1,5%) не наблюдалось. С экономической точки зрения целесообразно применять более дешевое сырье, или меньшую его количество. Поэтому целесообразнее применять гидролизаты побочных продуктов овсяной или ржаной муки с 0,5%-й концентрации сахаров. Поскольку стоимость сырья применялась в качестве источника углерода в контрольном (зеленая патока) и опытных средах (гидролизаты побочных продуктов муки) примерно одинакова, а выход биомассы на опытных средах увеличивается в 2 — 2,5 раза, поэтому гидролизаты побочных продуктов овсяного и ржаного муки можно предлагать в качестве источников углерода для глубинного промышленного культивирования гриба Pleurotus ostreatus с целью повышения выхода биомассы гриба качестве источника пищевого белка.
В проведенном исследовании осуществили подбор сырья, а именно источников и оптимальных концентраций азота, при одновременном применении гидролизатов побочных продуктов крупяной муки с концентрацией сахаров 0,5%, для процесса выращивания гриба Pleurotus ostreatus в глубинных условиях (табл.2).
Таблица 2 – Определение оптимальной концентрации глютена для выращивания гриба Pleurotus ostreatus на питательных средах с гидролизатами побочных продуктов овсяной и ржаной муки с концентрацией сахаров 0,5%
| Источники углерода и азота | Концентрация глютена,% | Количество сухой биомассы, г/100 мл * |
| Зеленая патока и кукурузный экстракт | — | 1,977 ± 0,098 |
| Овсяный гидролизат и глютен | 20 | 1,691 ± 0,084 |
| 30 | 4,339 ± 0,216 | |
| 40 | 5,329 ± 0,266 | |
| 50 | 4,643 ± 0,232 | |
| Ржаной гидролизат и глютен | 20 | 1,649 ± 0,082 |
| 30 | 4,488 ± 0,224 | |
| 40 | 5,281 ± 0,264 | |
| 50 | 4,973 ± 0,248 |
* — Данные представлены в виде x ± m • t0,05, где x — среднее арифметическое, m — ошибка среднего арифметического, t0,05 — коэффициент Стьюдента на уровне значимости 0,05.
При применении глютена в качестве источника азота, было определено, что 20% концентрация не дает увеличения биомассы отношении контроля, а другие исследовательские концентрации обеспечивают увеличение более чем в 2 раза по сравнению с контролем. Применение 30% концентрации глютена дает повышение количества биомассы примерно в 2,3 раза, 40% — в 2,7 раза по сравнению с контролем. Разница количества биомассы, полученной с применением глютена с концентрациями 30% и 40% составляет примерно 20% с приоритетом 40% концентрации глютена. Но с экономической точки зрения можно предлагать применять среды с 30% концентрацию глютена. При применении 50% концентрации глютена отмечено снижение количества биомассы до 15% по сравнению с 40% концентрацией глютена, что может быть связано с ухудшением массообмена в культуральной жидкости через его вязкую консистенцию. Таким образом, установлено, что применение глютена в концентрациях менее 30% и более 40% не обосновано. При применении гидролизатов побочных продуктов разных видов муки, с концентрацией сахаров 0,5%, достоверных различий не наблюдалось для всех исследовательских концентраций глютена.
Применение соевого молока в качестве источника азота, не дает однозначных результатов при использовании различных концентраций молока и различных видов гидролизатов побочных продуктов мукомольной промышленности (табл.3).
Таблица 3 – Определение оптимальной концентрации соевого молока для выращивания гриба Pleurotus ostreatus на питательных средах с гидролизатами побочных продуктов овсяной и ржаной муки с концентрацией сахаров 0,5%
| Источники углерода и азота | Концентрация соевого молока,% | Количество сухой биомассы, г/100 мл * |
| Зеленая патока и кукурузный экстракт | — | 1,977 ± 0,098 |
| Овсяный гидролизат и соевое молоко | 85 | 4,160 ± 0,208 |
| 50 | 3,201 ± 0,160 | |
| 20 | 2,103 ± 0,105 | |
| Ржаной гидролизат и соевое молоко | 85 | 3,083 ± 0,154 |
| 50 | 2,013 ± 0,100 | |
| 20 | 1,657 ± 0,082 |
* — Данные представлены в виде x ± m • t0,05, где x — среднее арифметическое, m — ошибка среднего арифметического, t0,05 — коэффициент Стьюдента на уровне значимости 0,05.
Применение 20%-го соевого молока дает выход биомассы аналогичен контролю, как для овсяной, так и ржаной гидролизатов. Соевое молоко с объемной концентрацией 50% вызвало увеличение количества биомассы, по сравнению с контролем, только на овсяной гидролизате (62%). Значение количества биомассы на ржаном гидролизате сравнимое с контролем. Использование 85%-го соевого молока способствовало накоплению биомассы гриба больше в 2 раза овсяной и в 1,5 на ржаном гидролизата, по сравнению с контролем.
Концентрация азота в контрольной среде (6% кукурузного экстракта) и опытных средах с глютеном (30%) или соевым молоком (50%) примерно одинакова и составляет 0,22-0,24%. Исследование соевого молока и глютена в качестве источников азота обнаружили, что при одинаковой концентрации азота целесообразно применять глютен независимо от вида муки (рис. 1).
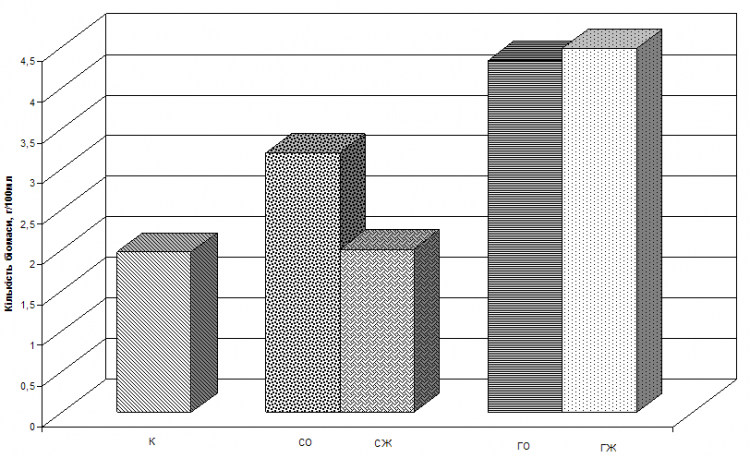
Рисунок 1 – Диаграмма зависимости количества биомассы гриба Pleurotus ostreatus от качества источников азота и вида гидролизата, при одинаковой концентрации азота (0,22-0,24%): К — кукурузный экстракт (6%), зеленая патока (5%) — контроль; СО — соевое молоко (50%), овсяный гидролизат (13%) СЖ-соевое молоко (50%), ржаной гидролизат (13%) ГО — глютен (30%), овсяный гидролизат (13%) ГЖ — глютен (30 %), ржаной гидролизат (13%).
При сравнении количества биомассы при применении глютена и соевого молока с одинаковыми концентрациями азота в овсяной и ржаной гидролизата, с концентрацией сахаров 0,5%, было выявлено преимущество глютена: примерно до 36% на овсяных гидролизата и примерно в 2 раза на ржаных гидролизат. Количество биомассы, что получено на средах с 85%-ным соевым молоком (концентрация азота — 0,43%) равно количеству биомассы, полученной на средах с 30%-ным глютеном (концентрация азота — 0,24%). То есть, увеличение количества азота в соевом молоке не приводит к ожидаемому увеличению количества биомассы. Однако, грибная биомасса, полученная в данных опытах при использовании овсяной гидролизата и соевого молока, имела выраженный грибной вкус и аромат, что не наблюдалось при применении других комбинаций источников углерода и азота. Это может свидетельствовать о том, что именно комбинация соевого молока и гидролизатов побочных продуктов овсяной муки способствует образованию грибного аромата в мицелии, полученного во время глубинного культивирования.
Таким образом, применение 85%-го соевого молока в качестве источника азота, при одновременном применении гидролизатов побочных продуктов овсяной муки, с концентрацией сахаров 0,5% дает возможность получать сухую биомассу мицелия в количестве примерно 40 г / л с выраженным грибным ароматом и вкусом . Применение глютена с концентрацией 30% в качестве источника азота, при одновременном применении гидролизатов побочных продуктов овсяной или ржаной муки, с концентрацией сахаров 0,5% дает возможность получать сухую биомассу мицелия в количестве примерно 40-50 г / л.
Заключение
Таким образом, для промышленного использования можно предложить применение глютена с концентрацией 30% в качестве источника азота, при одновременном применении гидролизатов побочных продуктов овсяной или ржаной муки, с концентрацией сахаров 0,5%, что дает возможность получать сухую биомассу мицелия в количестве примерно 40 — 50 г / л. Применение 85%-го соевого молока, в качестве источника азота, при одновременном применении гидролизатов побочных продуктов овсяной муки, с концентрацией сахаров 0,5% дает возможность получать сухую биомассу мицелия в количестве примерно 40 г / л. Но грибная биомасса, полученная при одновременном использовании овсяных гидролизатов и соевого молока, имеет весомые качественные преимущества, а именно грибной аромат и вкус. Вероятно, данная комбинация источников углерода и азота, обогащая питательную среду рядом аминокислот, способствует образованию грибного аромата и вкуса, что не противоречит литературным данным [5]. Результаты исследований показали возможность увеличения количества биомассы путем оптимизации питательной среды для глубинного культивирования промышленных штаммов вешенки. Перспективы последующих исследований в данном направлении заключается в дальнейшей оптимизации среды путем применения другой крахмалсодержащего сырья в качестве источника углерода.
Список литературы
- Пат. 2126835 РФ, кл. С12Р21/00, C12N1/14, C12R1/645. Способ получения белковой биомассы. / В. Ф. Колесникова, Д. А. Пцкиаладзе – №98104578/13; заявл. 25.03.98; опубл. 27.02.99; Бюл. №6.
- Пат. 2189395 С2 РФ, МПК C12P21/00, C12N1/14, C12R1/645. Способ получения белковой биомассы гриба. / М. Б. Биттеева и др. – №2000120039/13; заявл. 31.07.00; опубл. 20.09.02.
- Цизь О. М. Господарсько-біологічна оцінка штамів гливи звичайної / О. М. Цизь, Є. В. Лящук // “Наукові доповіді НАУ”, 2007. – Т. 3. – №8. – С. 20-27.
- Зубарева И. М. Глубинное культивирование высших базидиомицетов / И. М. Зубарева, О. В. Кузнецова // Вопросы химии и химической технологи, 2002. – №1. – С. 67-71.
- Формирование аромата сушеных шампиньонов / Т. А. Мишарина, С. М. Мухутдинова, Г. Г. Жарикова [и др.] // Прикладная биохимия и микробиология. – 2010. – Т.46. – №1. С. 119-124.
- Зубарева І. М. Порівняльна характеристика гібридного штаму Pleurotus ostreatus / Зубарева І. М., Федорова І. С., Лебедєва О. М. // Вопросы химии и химической технологи, 2005. – №3. – С. 74-78.
- Супрун-Крестова О. Ю. Технологія кормових добавок з використанням нетрадиційної сировини: автореф. дис. на здобуття наук. ступеня канд. техн. наук: спец. 05.18.02 «технологія зернових, бобових, круп’яних продуктів та комбікормів» / Супрун-Крестова Олена Юріївна; Нац. ун-т. харч. технол. – К., 2005. – 17 с.
- Тарабукин Д. В. Ферментативные технологии направленной биоконверсии целлюлозо- и крахмалсодержащего растительного сырья: автореф. дис. на здобуття наук. ступеня канд. биол. наук: спец. 03.00.23 «Биотехнология» / Тарабукин Дмитрий Валерьянович; Ин-т биологии Уфим. науч. центра РАН. – Уфа, 2009. – 23 с.
- Математичне моделювання та оптимізація об’єктів технології неорганічних речовин / Л.А. Фролова, Б.І. Мельников, Ю.Д. Галівець, Н.Б. Мітіна. – Дніпропетровськ: Журфонд, 2010. – 208 с.
Авторы статьи: Ляпустина Е.В., Зубарева И.М., Лебедева О.Н.
Автор фото в статье: Ляпустина Е.В.
