Витамины – группа низкомолекулярных органических веществ, которые в очень низких концентрациях оказывают сильное и разнообразное биологическое действие. В природе источником витаминов являются главным образом растения и микроорганизмы. Менахиноны и кобаламины синтезируются исключительно микроорганизмами. И хотя химический синтез в производстве большей части витаминов занимает ведущее положение, микробиологические методы также имеют большое практическое значение [1,2].
Принципы химического строения витаминов настолько разнообразны, что классификация их на основе структуры невозможна. Витамины делятся по принципу растворимости на жирорастворимые и водорастворимые. Из жирорастворимых витаминов наибольшее значение в народном хозяйстве и в микробиологической промышленности имеют витамины групп А и D, а из водорастворимых – витамины В2 и В12 [1,4]. Кроме того, микроорганизмы используются как селективные окислители сорбита в сорбозу (при получении витамина С), а также для производства витаминных концентратов (витамина В2, каротиноидов). Перспективно микробиологическое получение биотина, используемого в рационе кур и свиней. В настоящее время на Западе в большую часть комбикормов для свиней включают биотин, получаемый путем химического синтеза. В результате химического синтеза образуется рацемическая смесь, а биологическая активностью обладает лишь D-форма витамина, которую синтезируют микроорганизмы [1].
Витамин B12
Среди неполимерных соединений витамин B12 имеет самое сложное строение. Это α (5,6-диметилбензимидазол) – кобамидцианид:
В молекулевитамина B12 различают:
1. Порфириноподобное, хромофорное, или корриновое, кольцо, связанное с атомом кобальта четырьмя координационными связями через атомы азота.
2. Верхним координационным лигандом кобальта в витамине B12 является цианогруппа. Ее место могут занимать другие неорганические или органические заместители, например NO22-, SO22-, ОН—, H2O, CH3, аденозил; заместители определяют название производных витамина B12.
3. Шестая позиция кобальта занята нуклеотидным ядром (нижним лигандом кобальта), состоящим из азотистого основания, рибозы и остатка фосфорной кислоты. Нуклеотидное ядро связано с кобальтом через азот основания, а с корриновым кольцом через аминопропаноловый мостик.
В составе витамина B12 или цианкобаламина азотистое основание представлено 5,6-диметилбензимидазолом (5,6-ДМБ). Наличие 5,6-ДМБ определяет активность молекулы корриноидов (синоним названия витаминов группы B12) для высших животных. Вместо 5,6-ДМБ микроорганизмы могут включать в молекулу другие бензимидазольные и пуриновые основания. Нуклеотидное ядро вообще может отсутствовать, как в случае фактора В.
Через 25 лет после открытия витамина B12 в 1972 г. в результате многолетних исследований был осуществлен полный химический синтез корриноидной структуры. Корриноид синтезирован в результате тридцати семи последовательных ступеней, но в силу сложности такого синтеза микробиологический метод остается пока единственным промышленным способом получения витамина B12 [1].
Продуценты витамина B12
В природе витамин B12 и родственные корриноидные соединения находят в клетках микроорганизмов, в тканях животных и некоторых высших растениях (горох, лотос, побеги бамбука, листья и стручки фасоли). Однако происхождение витамина B12 в высших растениях окончательно не установлено. Такие низшие эукариоты, как дрожжи и мицелиальные грибы, корриноиды, по-видимому, не образуют. Организм животных не способен к самостоятельному синтезу витамина. Среди прокариот способность к биосинтезу корриноидов широко распространена. Активно продуцируют витамин В12 представители рода Propionibacterium [1, 4, 5].Природные штаммы пропионовокислых бактерий образуют 1,0-8,5 мг/л корриноидов, но получен мутант Р. shermaniiМ-82, с помощью которого получают до 58 мг/л витамина [1,5]. В семействе Propioni bacberiaceae есть и другие представители, способные к высокому накоплению витамина B12в клетках. Это, прежде всего Eubacterium limosum Butyribacterium rettgerii).Как продуценты витамина практический интерес имеют многие представители актиномицетов и родственных микроорганизмов [1, 4]. Истинный витамин B12 в значительных количествах синтезирует Nocardiarugosa. Путем мутаций и отбора получен штамм N. rugosa, накапливающий до 18 мг/л витамина B12. Активные продуценты витамина обнаружены среди представителей рода Micromonospora: M. purpureae, M. echinospora, M. halophitica, M. fusса, M. chalceae. Высокой кобаламинсинтезирующей активностью обладают метаногенные бактерии, например Methanosarcina barkeri, M. vacuolataи отдельные штаммы галофильного вида Methanococcus halophilus [1, 4].Последний организм синтезирует более 16 мг корриноидов на грамм биомассы. Столь высокого содержания корриноидов не отмечено ни у одного другого из изученных микроорганизмов. Причина высокого содержания корриноидов у метаногенных бактерий не установлена. Корриноиды синтезируют строго анаэробные бактерии из рода клостридий. У Clostridlum tetanomorphum и Cl. sticklandil аденозилкобаламин входит в состав ферментных систем, катализирующих специфические реакции изомеризации таких аминокислот, как глутаминовая, лизин и орнитин. В значительных количествах образуют витамин B12 ацетогенные клостридий Cl. thermoaceticum, Cl. formicoaceticum и Acetobacter woodi, синтезирующие ацетат из СО2. Известны активные продуценты витамина B12 у псевдомонад, среди которых лучше других изучен штамм Pseudomonas denitrificans MB-2436 – мутант, дающий на оптимизированной среде до 59 мг/л корриноидов. Интерес представляют термофильные бациллы, а именно Bacillus circulans и Вас. stearothermophilus, которые растут соответственно при 60 и 75 °С и за 18 ч. культивирования без соблюдения стерильных условий дают высокие (2,0-6,0 мг/л) выходы витамина. Корриноиды синтезируют Rhodopseudomonas palustris, фототрофные пурпурные бактерии Rhodobactersphericus, Rh. capsulatus, Rhodospirillumrubrum, Chromatiumuinosumи ряд других видов. Значительные количества витамина B12 образует цианобактерии Anabaena cylindrica, одноклеточные зеленые водоросли Chlorella pyrenoidosae и красные водоросли Rhodosorus marinus [1].
Питательные среды
Продуценты витамина B12 культивируют в средах, приготовленных на основе пищевого сырья: соевой муки, рыбной муки, мясного и кукурузного экстракта. В последние годы выявлены микроорганизмы, образующие высокие качества корриноидов при утилизации непищевого сырья. Achromobactersp., используя изопропиловый спирт как источник углерода и энергии, накапливает до 1,1 мг/л провитамина, Pseudomonassp. синтезирует витамин B12 в среде с метанолом или пропандиолом (до 160 мкг/л), факультативный метилотроф образует в среде с метанолом до 2,6 мг/л витамина. Выделен штамм Klebsiella 101, образующий большое количество корриноидов в клетках только при росте на среде с метанолом как единственном источнике углерода и энергии [1].
Биосинтез витамина В12 [1]:
Производство витамина В12
В нашей стране в качестве продуцента витамина В12 используют Propionibacteriumf reudenreichii var. Shermanii [1,5].Для получения витамина B12 бактерии культивируют периодическим методом в анаэробных условиях в среде, содержащей кукурузный экстракт, глюкозу, соли кобальта и сульфат аммония. Образующиеся в процессе брожения кислоты нейтрализуют раствором щелочи, которая непрерывно поступает в ферментер. Через 72 ч в среду вносят предшественник – 5,6-ДМБ. Без искусственного введения 5,6-ДМБ бактерии синтезируют фактор В и псевдовитаминB12 (азотистым основанием служит аденин), не имеющие клинического значения. Ферментацию заканчивают через 72 ч. Витамин B12 сохраняется в клетках бактерий. Поэтому после окончания брожения биомассу сепарируют и экстрагируют из нее витамин водой, подкисленной до рН 4,5-5,0 при 85-90 С в течение 60 мин с добавлением в качестве стабилизатора 0,25%-ной NaNO2. При получении Ko-B12 стабилизатор не добавляют. Водный раствор витамина B12 охлаждают, доводят рН до 6,8-7,0 50%-ным раствором NaOH. К раствору добавляют Аl2(SO4)3*18H2Oи безводный FеСl3 для коагуляции белков и фильтруют через фильтр-пресс. Очистку раствора проводят на ионообменной смоле СГ-1, с которой кобаламины элюируют раствором аммиака. Далее проводят дополнительную очистку водного раствора витамина органическими растворителями, упаривание и очистку на колонке с Al2O3. С окиси алюминия кобаламины элюируют водным ацетоном. При этом Ko-B12 может быть отделен от CN- и оксикобала мина. К водно-ацетоновому раствору витамина добавляют ацетон и выдерживают при 3-4°С 24-48 ч. Выпадающие кристаллывитамина отфильтровывают, промывают сухим ацетоном и серным эфиром и сушат в вакуум-эксикаторе над P2O5. Для предотвращения разложения Ko-B12 все операции необходимо проводить в сильно затемненных помещениях или при красном свете. Таким образом, можно получить не только смесь CN- и оксикобаламинов, но и коферментную форму, которая обладает высоким терапевтическим эффектом. Для химической очистки витамина B12 используется его способность образовывать продукты с фенолом и резорцином. При этом способе отделение витамина B12от сопутствующих ему факторов упрощается. Промышленный концентрат цианкобаламина обрабатывают водным раствором резорцина (или фенола), выделяют комплекс витамина B12 с резорцином (или фенолом), далее разлагают его и получают кристаллический препарат [1].
Применение витамина В12
Для обогащения кисломолочных продуктов витамином B12 используют пропионовокислые бактерии как в чистом виде, таки в виде концентрата, приготовленного на молочной сыворотке. Для нужд животноводства витамин B12 получают, используя смешанную культуру, содержащую термофильные метанообразующие бактерии [1,4]. Установлено образование корриноидов не только в смешанной, но и в чистой культуре метан образующих бактерий Methanosarcina barkeri, Methanobacterium formicum, Mb. thermoautotrophicum при росте в присутствии H2 и CO2. Содержание корриноидов у метанобразующих бактерий составляет 1,0-6,5 мг/г сухой биомассы. С помощью смешанной культуры метанобразующих бактерий разработан метод получения кормового препарата витамина B12-KMБ12. Субстратом для метанового брожения служит ацетоно-бутиловая и спиртовая барда. Ацетоно-бутиловую барду получают в результате удаления растворителей из культуральной жидкости Clostridium acetobutylicum, сбраживающей паточно-мучные заторы. Для метанового брожения используют декантат барды, содержащий 2,0-2,5 %сухих веществ. К декантированной барде добавляют 4 г/м3 СоСl2 и 0,5% метанола как стимуляторы синтеза кобаламинов. В качестве биостимуляторов вносят также карбамид и диаммонийфосфат, 5,6-ДМБ не вносят, поскольку CN=B12и фактор III, обладающие биологической активностью, составляют до 80% от суммы всех корриноидов. Исходная барда имеет температуру около 100°С и практически стерильна. Перед поступлением в ферментеры барда охлаждается до 55-57°С. В качестве исходной культуры используют смешанную культуру метанообразующих бактерий, осуществляющих термофильное «метановое брожение» сточных вод. Получение концентрата витамина B12включает следующие технологические стадии: непрерывное сбраживание барды комплексом бактерий, сгущение метановой бражки и сушку сгущенной массы на распылительной сушилке [1,4]. Брожение проводят в железобетонных ферментерах непрерывным способом в течение года. Важное условие нормального процесса брожения – контроль уровня жирных кислот и аммонийного азота. Витамин B12 неустойчив при тепловой обработке, особенно в щелочной среде. Поэтому перед выпариванием к метановой бражке добавляют – Cl до оптимального значения рН 5,0-5,3 и сульфит Na(оптимальное содержание 0,07-0,1%). Перед поступлением на установку выпаривания метановая бражка дегазируется путем нагревания до 90–95°С при атмосферном давлении. Бражку сгущают до 20% сухих веществ в четырехкорпусных выпарных аппаратах. Сгущенная метановая бражка высушивается на распылительной сушилке.
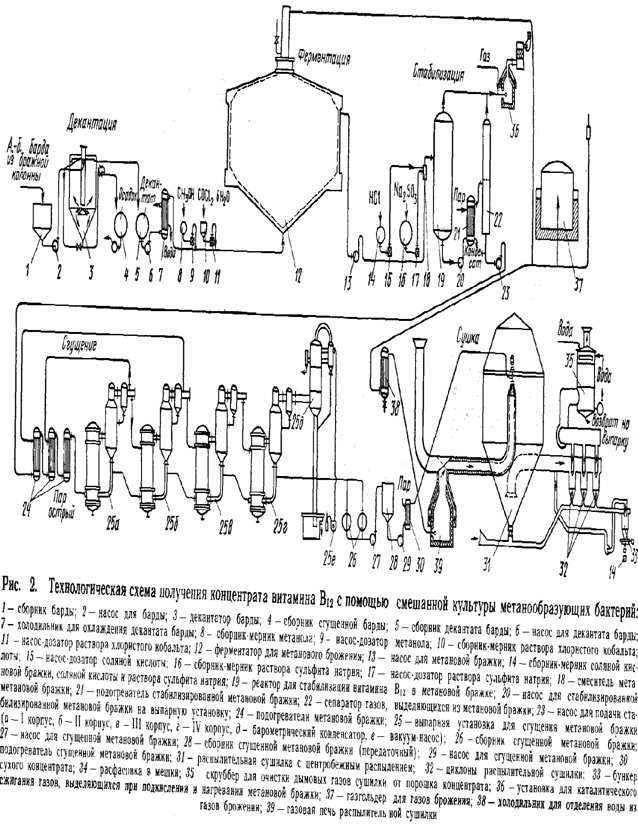
Технологическая схема представлена на рисунке. Ацетоно-бутиловая барда из нижней части бражной колонны поступает в сборник барды и насосом подается в декантатор 3. Отстой барды собирается в сборнике 4 и используется на корм скоту. Декантат, охлажденный до температуры 55-57°С, метанол и хлористый кобальт поступают в ферментер 12. Сброшенную массу из верхней части ферментера отбирают и направляют в реактор 19, где осуществляют стабилизацию витамина B12путем добавления сульфита натрия и соляной кислоты, смешанных в смесителе 18. Из стабилизированной бражки удаляют газы в сепараторе газов 22, бражку упаривают в выпарной установке 24 и собирают в сборниках 26. Сгущенная метановая бражка перекачивается насосом 27 в сборник метановой бражки 28, а от туда насосом 29 в распылительную сушилку 31. В качестве теплоносителя для сушки используют газы брожения, сжигаемые в печи 39. Сухой порошок поступает в бункер 33 и расфасовывается в полиэтиленовые мешки, вложенные в крафт-пакеты. Отсутствие промышленных отходов, доступность сырья, непрерывность метода, не требующего стерильных условий, делают его экономичным [1].
Украинским научно-исследовательским институтом спиртовой и ликеро-водочной промышленности разработана технология получения кормового концентрата витамина B12 путем сбраживания мелассно-спиртовой барды смешанной культурой метанообразующих бактерий. Предварительно на мелассно-спиртовой барде выращивают кормовые дрожжи. После сепарирования дрожжей получают культуральную жидкость, содержащую 7-8% сухих веществ. На этой жидкости выращивают метанообразующие бактерии и получают с 1 м3 исходной барды 1,5-2 г витамина В12 [1].
Список литературы
- Промышленная микробиология: Учеб. пособие для вузов П 81 по спец. “Микробиология” и “Биология” / З.А.Аркадьева, А.М. Безбородов, И.Н.Блохина и ДР.; Под ред.. Н.С. Егорова. – М.:Высш. шк., 1989. – 688 с.: ил.
- Н.А. Шмалько, И.И. Уварова, Ю.Ф. Осляков. Амарантовая мука – антиоксидантная добавка для макаронных изделий, обогащенных β–каротином // Пищевая технология. – 2004г. – №5–6. – стр. 39–41.
- К.К. Полянский, Л.В. Голубева, О.И. Дол матова, Д.В. Дорохина. Изучение реологических свойств видов молочных консервов с β–каротином // Пищевая технология. – 2001г. – №1. – стр. 28–29.
- Никтин Г.А. Биохимические основы микробиологических производств: Учеб. пособие. – Киев: Вища школа. Головное изд-во, 1981. – 312 с.
- Елинов Н.П. Основы биотехнологии. Издательская фирма “Наука” СПБ 1995г. 600 стр. 166 ил.
- Голубев В.Н., Жиганов И.Н. Пищевая биотехнология. – М.: ДеЛи принт, 2001. – 123 с.
Читайте также статьи по теме «Производство витаминов»:
- Производство витамина D
- Производство витамина рибофлавина
- Производство витамина С
- Производство витаминов
- Бета-каротин и витамин А
Автор статьи и фото в статье: Ляпустина Е.В.
