Влияние экзогенных регуляторов роста на индукцию каллусогенеза в культуре тканей Clematis vitalba
Одним из важных этапов создания клеточных культур – продуцентов вторичных метаболитов является оптимизация условий индукции каллусогенеза. Данный этап предполагает дедифференциацию клеток экспланта, выход их из-под контроля интегрирующих систем организма и дальнейшее неограниченное внутренними и внешними факторами размножение. Среди факторов, влияющих на способность экспланта к каллусообразованию, выделяют биотические (физиологическое состояние экспланта, его генотип и эпигеном (цитоплазмон)) и абиотические (присутствие в питательной среде экзогенных регуляторов роста, сахарозы, наличие травматического воздействия, интенсивность освещения, влажность воздуха, температура в культуральной комнате и т.д.) [11, 43, 93, 116, 136, 172, 173].
Накопленные данные свидетельствуют о том, что для интенсификации индукции каллусогенеза и получения клеточных и тканевых культур исследователи наиболее часто используют модификацию имеющихся базовых питательных сред по составу регуляторов роста. В большинстве известных работ для получения каллусных культур используется эмпирический подбор регуляторного состава питательных сред, основным недостатком которого является некоторая несистемность используемых вариантов, что может, в конечном итоге, привести к некорректной оценке полученных результатов [8, 9, 11, 21, 43, 84, 85, 93, 108, 116, 136, 172, 173].
Одним из подходов к оптимизации питательных сред для индукции каллусогенеза является выявление закономерностей активации процессов каллусообразования на питательных средах, содержащих экзогенные регуляторы роста в широком диапазоне концентраций.
С этой целью экспланты из вегетативных органов C. vitalba (почек и молодых листьев) культивировали на модифицированных питательных средах В5 и LS, различающихся по содержанию макро- и микроэлементов, витаминов, сахарозы и регуляторов роста – 2,4-Д и БАП. Концентрация регуляторов роста в средах соответствовала матрице планирования эксперимента (табл. 1). Минимальная концентрация и «шаг» изменения концентраций регуляторов роста составляли 0,5 мг/л. Низкие концентрации 2,4-Д на фоне более высоких концентраций БАП в данном эксперименте не анализировали, так как последние могли приводить к процессам регенерации, а не индукции каллусообразования.
Путем построения графической зависимости между частотой каллусообразования и регуляторным составом питательной среды удалось выявить закономерности каллусообразования под воздействием регуляторов роста. Результаты исследований по индукции каллусообразования иллюстрируются графиками, представленными на рисунках 1 и 2.
Таблица 1 — Матрица планирования эксперимента по оптимизации состава питательной среды для индукции каллусообразования извегетативных эксплантов Clematis vitalba
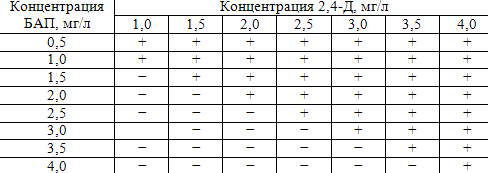
+ — анализируемые варианты концентраций регуляторов роста
− — не анализируемые варианты сочетания регуляторов роста
Культивирование эксплантов на модифицированных питательных средах В5 показало, что зависимость частоты каллусообразования от концентрации регуляторов роста носила сложный нелинейный характер (рис. 1). Высокие значения показателя частоты каллусообразования наблюдались в довольно широком диапазоне концентраций 2,4-Д и БАП.
Максимальная частота каллусообразования (97 %) была отмечена при концентрациях 2,4-Д и БАП 1,5 мг/л. Высокие показатели частоты каллусообразования (в пределах 93-95 %) наблюдали на средах, содержащих указанные регуляторы роста в концентрациях 3,0 мг/л и 3,5 мг/л, а также на средах, дополненных 4,0 мг/л 2,4-Д и 3,5 мг/л БАП.
Частота каллусообразования в пределах 80-90 % отмечена на средах, дополненных регуляторами роста в следующих концентрациях:
- 3,5 мг/л 2,4-Д и 3,0 мг/л БАП – 88 %;
- 1,0 мг/л 2,4-Д и 0,5 мг/л БАП – 86 %;
- 3,0 мг/л 2,4-Д и 2,5 мг/л БАП – 83 %;
- 1,5 мг/л 2,4-Д и 1,0 мг/л БАП – 80 %;
- 3,5 мг/л 2,4-Д и 2,0 мг/л БАП – 80 %.
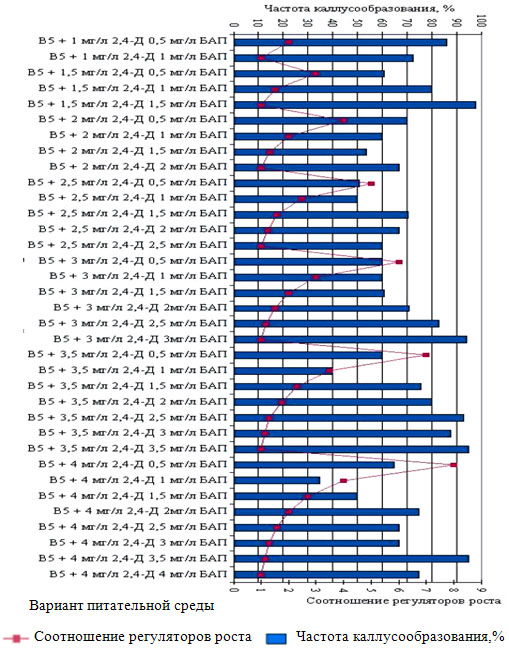
Рисунок 1 — Зависимость частоты каллусообразования в культуре вегетативных органов C. vitalba от соотношения концентраций регуляторов роста в модифицированных питательных средах В5
Частоту каллусообразования на уровне 70-75 % наблюдали на питательных средах, содержащих:
- 3,5 мг/л 2,4-Д и 1,5 мг/л БАП;
- 2,0 мг/л БАП и 4,0 мг/л 2,4-Д;
- 4,0 мг/л БАП и 4,0 мг/л 2,4-Д.
При культивировании эксплантов на других модификациях питательной среды В5 показатель частоты каллусообразования находился в пределах от 50 до 70 %. Только на 2-х из 35-ти вариантов питательных сред были отмечена частота каллусообразования ниже 50 % – на среде, дополненной 3,5 мг/л 2,4-Д и 1,0 мг/л БАП; и на среде, содержащей 4,0 мг/л 2,4-Д и 1,0 мг/л БАП.
На рисунке 2 представлен график, иллюстрирующий зависимость частоты каллусообразования от содержания регуляторов роста в питательной среде при культивировании эксплантов на модифицированных питательных средах LS. Из данных, представленных на графике, видно, что, как и в случае модификации сред В5, зависимость частоты каллусообразования от гормонального состава носила нелинейный характер.
Однако следует отметить, что общий уровень частоты каллусообразования при культивировании на этой среде был ниже. Максимальные показатели частоты каллусообразования (95 %) отмечены на двух модификациях среды LS, содержащей по 2,0 мг/л 2,4-Д и БАП, а также 3,5 мг/л 2,4-Д и 2,0 мг/л БАП.
Высокие показатели частоты каллусообразования – на уровне около 80 % выявлены на питательных средах, дополненных:
- 1,5 мг/л 2,4-Д и 1,5 мг/л БАП;
- 2,5 мг/л 2,4-Д и 2,0 мг/л БАП;
- 3,0 мг/л 2,4-Д и 1,5 мг/л БАП.
Частота каллусообразования на уровне 70-75 % отмечана на 3-х модификациях среды LS, дополненных:
- 4,0 мг/л 2,4-Д и 3,5 мг/л БАП;
- 4,0 мг/л 2,4-Д и 2,0 мг/л БАП;
- 4,0 мг/л 2,4-Д и 3,0 мг/л БАП.
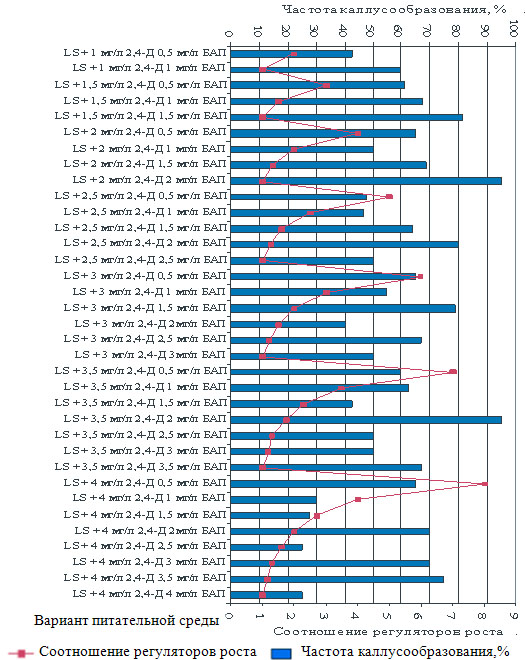
Рисунок 2- Частота каллусообразования в культуре вегетативных органов C. vitalba от соотношения концентраций регуляторов роста в модифицированных питательных средах LS
При культивировании эксплантов на 12-ти других модификациях питательных сред LS частота каллусообразования составила 60 %. Для остальных модификаций показатель частоты каллусообразования не превышал 50 %. Низкие показатели частоты каллусообразования (менее 40 %) выявлены на 9-ти питательных средах.
Таким образом, проведенные нами исследования показали возможность получения каллусных культур из вегетативных органов ломоноса виноградолистного на модифицированных питательных средах В5 и LS, дополненных 2,4-Д и БАП в широком диапазоне концентраций.
Полученные данные подтверждают тот факт, что в культуре in vitro одним из определяющих факторов, влияющих на способность эксплантов к каллусообразованию, является наличие в питательной среде регуляторов роста, а минеральный и органический состав среды культивирования имеет второстепенное значение [153]. Кроме того, проведенные исследования продемонстрировали, что в культуре тканей C. vitalba, независимо от минерального состава питательной среды, наблюдается сходная картина по частоте каллусообразования в зависимости от соотношения регуляторов роста. При анализе полученных экспериментальных данных (рис. 3.2, 3.3) нами отмечено, что более высокие показатели частоты каллусообразования наблюдались при использовании невысоких концентраций регуляторов роста (в пределах 0,5-1,5 мг/л) при соотношении 2,4-Д:БАП, равном 2 (2,4-Д 1 мг/л и БАП 0,5 мг/л), или 1,5 (2,4-Д 1,5 мг/л и БАП 1,5 мг/л). Понижение или повышение коэффициента соотношения регуляторов роста до значений ниже или выше этого значения подавляло способность к каллусообразованию (например, 1,5 мг/л 2,4-Д и 0,5 мг/л БАП; 2,0 мг/л 2,4-Д и 0,5 мг/л БАП).
При использовании концентраций регуляторов роста в пределах 2,5-4,0 мг/л имела место обратная зависимость – при более низких (2/1, 1/1) значениях соотношения 2,4-Д:БАП частота каллусообразования снижалась, а при более высоких (7/1, 5/1) – повышалась. Высокие показатели частоты каллусообразования отмечены только при определенных соотношениях концентраций регуляторов роста. Так, высокий показатель частоты каллусообразования был отмечен при культивировании эксплантов на модификациях питательных сред с соотношением 2,4-Д:БАП, равном или близким к 1: 3,5 мг/л 2,4-Д+3,5 мг/л БАП; 4,0 мг/л 2,4-Д+3,5 мг/л БАП. При увеличении соотношения 2,4-Д:БАП показатель частоты каллусообразования был значительно ниже. Аналогичная закономерность была показана ранее и для других видов растений [89, 90].
Полученные результаты показали, что использованная нами 2,4-Д является основным дедифференцирующим фактором, способствующим индукции каллусообразования в культуре вегетативных органов C. vitalba. Однако для повышения частоты каллусообразования необходимо дополнительное введение в состав среды БАП.
Возможно, такое поведение эксплантов можно объяснить тем, что влияние различных концентраций регуляторов роста в совокупности с раневым воздействием при вычленении экспланта и составом среды культивирования является эффектором (триггером) переключения программы развития с органогенеза на каллусообразование, то есть имеет место смешанный тип регуляции процесса каллусообразования – с выраженной генетической составляющей способности к каллусообразованию – экспланты должны быть адекватны к восприятию гормонального сигнала, а внешняя среда содержить все элементы для развития такого ответа [21, 91, 172].
Из двух использованных минеральных основ для индукции каллусообразования по результатам проведенных исследований рекомендуется использовать среду по прописи В5, так как показатели частоты каллусообразования на данной среде были несколько выше, чем на среде по прописи LSчто, возможно, связано с генетической детерминированностью процессов каллусообразования. Выявленная закономерность может быть связана и с тем, что на среде В5 компетенция эксплантов к каллусообразованию повышается благодаря более высокому содержанию в питательной среде источников углеродного питания, макро- и микроэлементов.
Следует отметить, что содержание регуляторов роста, в пределах до 3,5 мг/л оказывало стимулирующее влияние на процессы дедифференциации и каллусогенеза, а выше 3,5 мг/л – частично ингибировало процессы каллусообразования.
Таким образом, основным фактором, определяющим процесс каллусообразования в культуре вегетативных почек, физиологически молодых и зрелых листьев C. vitalba,являлась концентрация и соотношение гормональных добавок в питательной среде, что говорит об их определяющем влиянии в индукции каллусогенеза для данного вида.
Ссылки на литературу в тексте соответствуют источнику Индуцированный морфогенез in vitro и накопление тритерпеновых гликозидов в каллусных культурах ломоноса виноградолистного (Clematis vitalba L.)
Источник: Сидякин А.И., Индуцированный морфогенез in vitro и накопление тритерпеновых гликозидов в каллусных культурах ломоноса виноградолистного (Clematis vitalba L.): Дис. … канд. биол. наук. Симферополь. 2011. – 217 с.
Автор фото в статье: Ляпустина Е.В.
Материал любезно предоставил Сидякин Андрей Иванович – к.б.н., ас. каф. ботаники и физиологии растений и биотехнологий и м.н.с. Биотехнологического центра НИЧ Таврического национального университета им. В.И. Вернадского, научный консультант ООО КрымБио
